
北京清华长庚医院3月20日电(供稿肝胆胰中心)肝细胞癌(Hepatocellular Carcinoma, HCC)以显著的纤维沉积和免疫抑制为特征性病理表现,尽管免疫检查点抑制剂(Immune Checkpoint Blockade, ICB)已成为晚期HCC的一线治疗方案,但客观缓解率仍不足30%,免疫耐药问题亟待突破。作为肝脏特有的间质细胞,肝星状细胞在肿瘤微环境中可极化为具有显著表型异质性的肿瘤相关成纤维细胞(Cancer Associated Fibroblasts, CAFs),其分泌的大量胶原纤维及细胞外基质交联产物为免疫细胞的浸润构筑了强大的屏障阻力。然而,HCC中CAFs的亚型异质性、空间分布规律及其在免疫耐药中的具体分子机制,仍缺乏高分辨率系统解析。
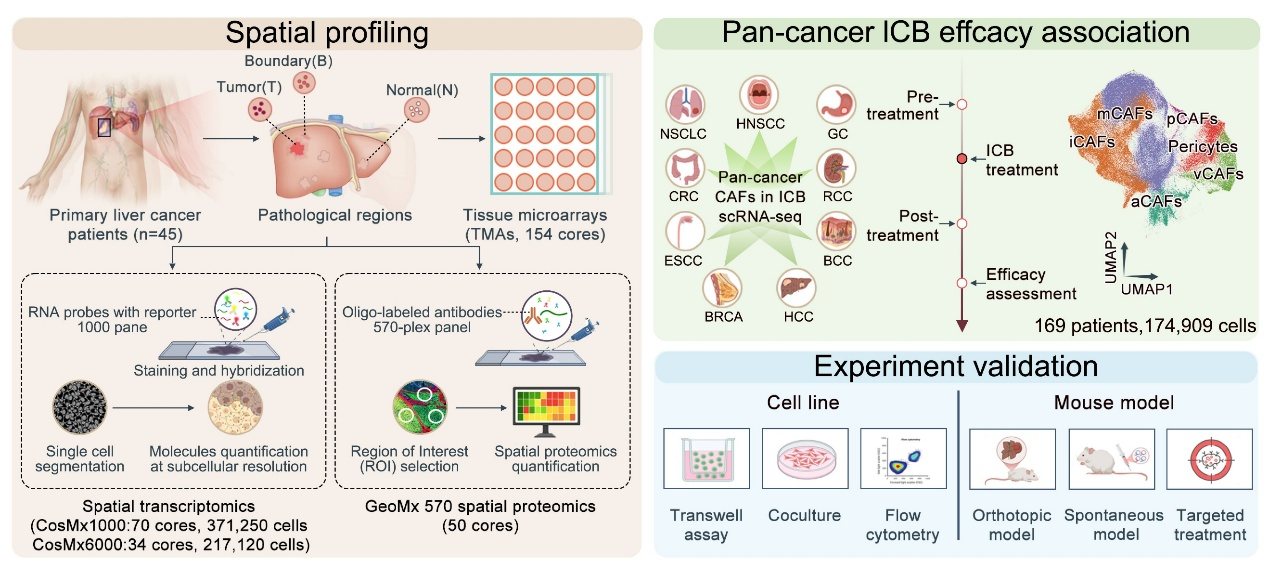
近日,清华大学北京清华长庚医院院长、肝胆胰中心董家鸿院士,肝脏外科副主任杨世忠团队依托CosMx SMI空间多组学技术,结合团队自主构建的泛癌免疫治疗单细胞转录组数据库scICB,系统解析了46例原发性HCC患者肿瘤实质区、侵袭前沿区及癌旁区的空间分子景观,首次在空间尺度上揭示了NOTCH3信号轴在肝癌纤维沉积与免疫治疗抵抗中的核心调控作用。
研究发现,HCC微环境中的CAFs呈现显著的功能极化与空间分层特征,其中炎症型CAFs(iCAFs)与基质生成型CAFs(mCAFs)构成两大主要亚群。mCAFs主要富集于肿瘤实质及侵袭前沿区域,与胶原沉积增强、免疫细胞排斥及不良预后显著相关;而iCAFs则更多分布于癌旁区域,与相对有利的预后相关。进一步结合团队前期开发的泛癌种单细胞转录组数据库scICB中超过300例患者、800余份免疫治疗样本的单细胞测序数据分析后发现,mCAFs富集显著关联免疫治疗耐药,而iCAFs比例升高则与临床应答密切相关。
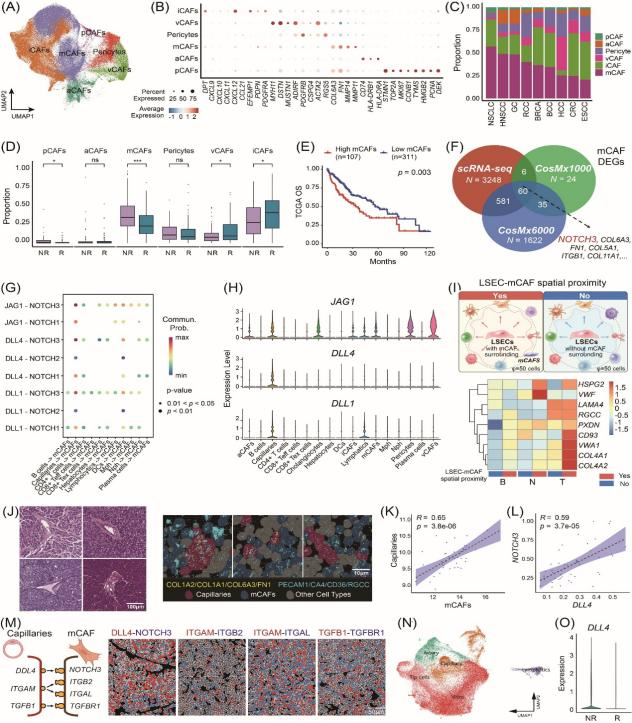
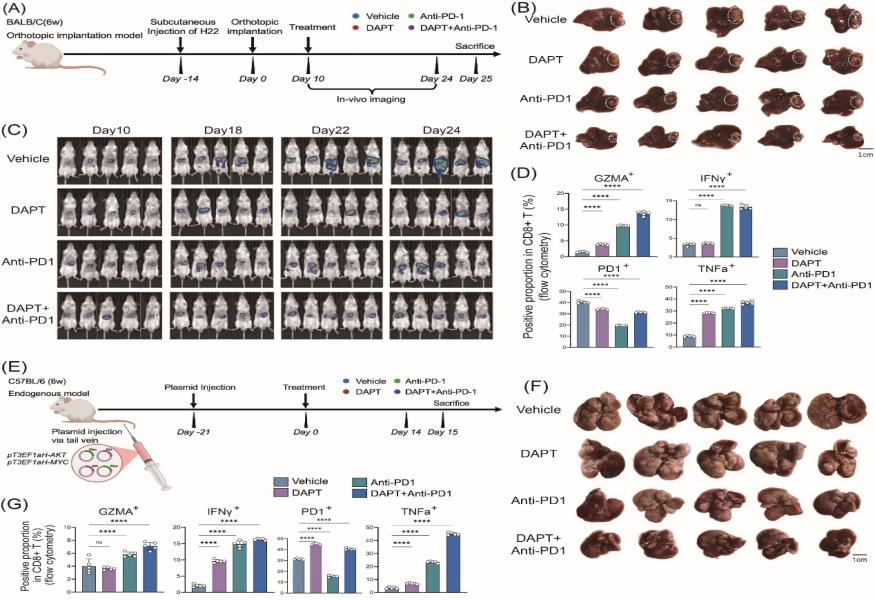
机制解析发现NOTCH3是驱动mCAFs胶原极化及纤维沉积的关键分子。空间距离约束的配受体互作分析显示,肝窦毛细血管来源的DLL4与mCAFs高表达的NOTCH3形成高度的空间共定位,构成特异性血管–成纤维细胞信号互作单元。DLL4–NOTCH3信号轴的激活促进细胞外基质重塑与胶原交联,增强组织刚度,形成物理和信号双重屏障,阻断CD8⁺ T细胞向肿瘤核心区域的有效浸润。体外功能实验显示,抑制NOTCH3可显著降低纤维化表型,增强CD8⁺ T细胞迁移及效应杀伤活性。在原位移植肝癌模型及自发性肝癌小鼠模型中,NOTCH通路抑制剂有效打破纤维屏障,显著提升肿瘤内T细胞浸润水平,并与抗PD-1治疗形成显著协同,大幅降低肿瘤负荷。
本研究在基础机制与临床转化层面具有重要的创新价值:
1. 突破了肝癌空间微环境解析的局限:以超高分辨率系统刻画了HCC肿瘤微环境的纤维沉积和免疫逃逸景观,突破了以往研究对侵袭前沿区等关键区域细胞组成和空间定位认识不清、分辨率不足的局限性,为后续研究肿瘤微环境的细胞互作提供了高分辨率的参考体系;
2. 揭示了肝癌免疫排斥的全新分子机制:明确了DLL4-NOTCH3调控肝窦毛细血管-mCAFs互作的分子轴线,将血管信号介导的纤维化与免疫排斥关联起来,为理解肝癌免疫耐药的核心机制提供了新的视角;
3. 提供了可转化的肝癌免疫治疗新策略:证实靶向NOTCH3与抗PD-1疗法的协同作用,为构建“抗纤维化 + 免疫治疗”联合治疗新模式提供了直接的实验依据与潜在靶点。
相关成果以Spatial multi-omics identifies a NOTCH3-mediated capillary–mCAF crosstalk driving immune exclusion in hepatocellular carcinoma(《空间多组学揭示NOTCH3介导的肝窦毛细血管–mCAF互作驱动肝细胞癌免疫排斥》)为题,发表在 iMeta (《宏》)上。本研究由北京清华长庚医院肝胆胰中心与病理科合作完成,董家鸿为本文首席通讯作者,肝胆胰中心科研型博士后季凡森、卓越医师科学家八年制项目李昊辰、肝胆胰中心科研型博士后王琪为本文共同第一作者。研究得到了国家自然科学基金重大项目、清华大学精准医学自主科研计划等项目的支持。病理科主任尹洪芳、主治医师肖颖、副主任技师杨江辉、全体技师组、华中科技大学同济医学院徐传瑞教授团队、中国医学科学院肿瘤医院高亦博教授团队对本研究亦有重要贡献。
原文链接: https://onlinelibrary.wiley.com/doi/10.1002/imt2.70117

北京清华长庚医院APP
快速挂号